鹼金屬檢視原始碼討論檢視歷史
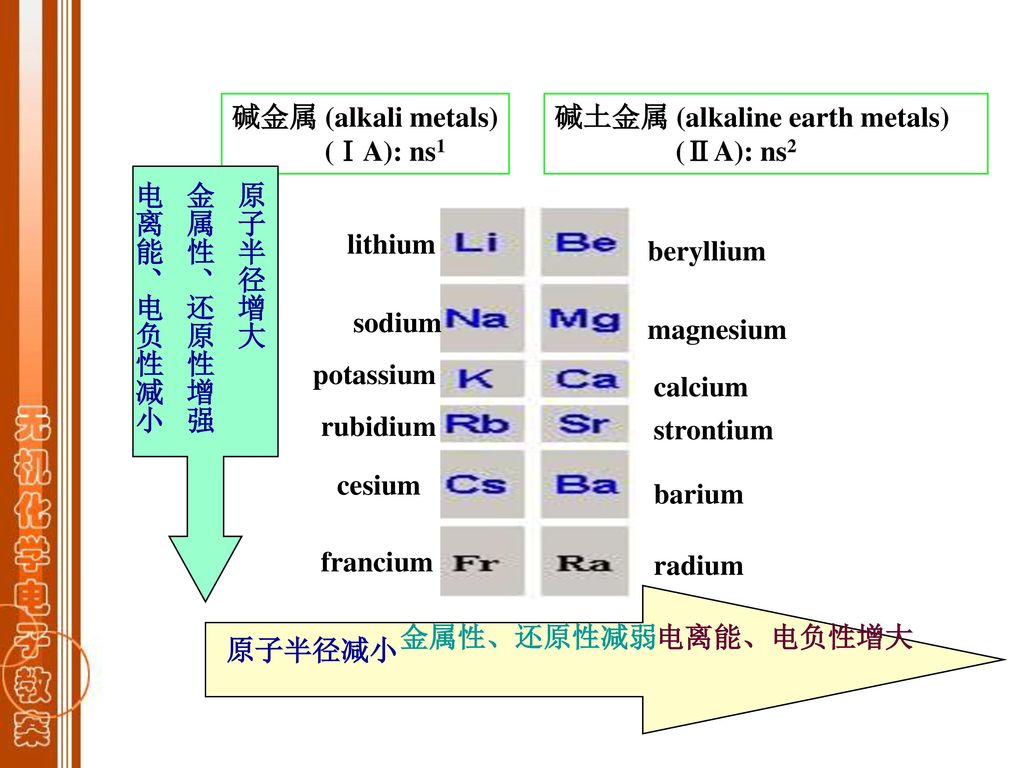 |
鹼金屬是指在元素周期表[1] 中同屬第1族(舊稱ⅠA族)的六個金屬元素:鋰(Li)、鈉(Na)、鉀(K)、銣(Rb)、銫(Cs)、鈁(Fr),其中鍅具有強烈的放射性。
鹼金屬均有一個屬於s軌道的最外層電子,,因此這一族屬於元素周期表的s區。鹼金屬的化學性質顯示出十分明顯的同族元素相似性,是化學元素周期性|periodic trends的例證之一。儘管氫也同屬於第1族,但其顯現的化學性質和鹼金屬相差甚遠,因此通常不被認為是鹼金屬。
鹼金屬有很多相似的性質;都是銀白色的金屬、密度小、熔點和沸點都比較低、標準狀況下有很高的反應活性|reactivity (chemistry)。它們易失去價電子形成帶一個單位正電荷的陽離子。它們一般質地較為柔軟,可以用刀切開,露出銀白色的剖面;由於能和空氣中的氧氣反應,剖面暴露於空氣中將很快失去光澤。由於鹼金屬化學性質都很活潑,貯存時一般將它們放在礦物油中,或封於稀有氣體中保存,以防止其與空氣或水發生反應。在自然界中,鹼金屬元素只有化合態,不能以穩定單質形式存在。鹼金屬都能和水發生激烈的反應,生成鹼性的氫氧化物,其反應能力與劇烈程度隨着原子序數的增大而越強。
所有已發現的鹼金屬均天然存在於自然界中。按照化學元素豐度順序,自然界化學豐度最高的是鈉,其次是鉀,接下來是鋰、銣、銫,最後是鈁。鈁的放射性很強,半衰期很短,十分不穩定,因此只能作為天然衰變鏈的產物,在自然界中痕量存在。已有實驗試圖合成可能的第七個鹼金屬Uue,但截至目前均以失敗告終。此外,由於相對論效應會極大影響包括Uue在內的超重元素的性質,因此Uue可能不是鹼金屬;即使它真的是鹼金屬,它的物理性質和化學性質也可能會和其它六個鹼金屬有較大差異。
鹼金屬有多種用途。銣或銫的原子鐘是游離態鹼金屬元素最著名的應用實例之一,其中以銫原子鐘最為精準。鈉化合物較為常見的一種用途是製作鈉燈,一種高效光源。人類對食鹽(氯化鈉)的使用可追溯到古代。鈉和鉀是生物體中的電解質,具有重要的生物學功能,屬於膳食礦物質。儘管其它鹼金屬並非膳食礦物質,它們同樣會對身體產生或有益或有害的影響。
性質
化學性質
鹼金屬元素的樣品,保存在礦物油中以防氧化。從左至右:鋰、鈉、鉀、銣、銫 這一族的核外電子結構(特別是最外層電子)模式特殊,因此它們的化學性質呈規律性變化:
| Z | 元素 | 核外電子構型 | 電子排布 |
|---|---|---|---|
| 3 | 鋰 | 2, 1 | [He] 2s1 |
| 11 | 鈉 | 2, 8, 1 | [Ne] 3s1 |
| 19 | 鉀 | 2, 8, 8, 1 | [Ar] 4s1 |
| 37 | 銣 | 2, 8, 18, 8, 1 | [Kr] 5s1 |
| 55 | 銫 | 2, 8, 18, 18, 8, 1 | [Xe] 6s1 |
| 87 | 鈁 | 2, 8, 18, 32, 18, 8, 1 | [Rn] 7s1 |
由於具有強烈的放射性,鈁可展現的的化學性質十分有限,因此它的化學性質並未得到深入研究。對鹼金屬元素的化學性質研究主要針對這一族的前五個元素。
已知的鹼金屬元素均為活潑金屬,至今尚未發現鹼金屬的天然單質。因此,鹼金屬通常泡在礦物油或煤油中保存。鹼金屬和鹵素劇烈反應生成鹵化物,為白色的離子晶體,除氟化鋰外均可溶於水。鹼金屬和水反應生成強鹼性的氫氧化物溶液,因此應當妥善保存。原子量越大(越「重」)的鹼金屬,反應越為劇烈:比如銫加入水中引發的爆炸比鉀更劇烈,就是一個例子。
由於擁有較低的有效核電荷,且只需失去一個電子就能達到稀有氣體電子結構,鹼金屬元素的第一電離能是同周期元素中最低的。與之相對的是,鹼金屬的第二電離能普遍很高,因為失去一個電子的鹼金屬離子為稀有氣體電子結構,而且電子和原子核的距離下降了。這一能量差異導致鹼金屬在反應中通常失去一個電子,形成一價正離子。
化學家起初認為鹼金屬不會形成負離子,但後來的研究發現了一類含負一價鹼金屬離子的不穩定化合物,稱作鹼化物。鹼化物中的鹼金屬負離子有充滿的s亞層,這使得它更加穩定。「反氫化鈉」,H+Na-,是這類化合物中一個引入注目的例子。通常的氫化鈉應當是Na+H-,反氫化鈉具有與之相反的電荷分布。因此,反氫化鈉的能量高,純淨物很不穩定,但它的幾種衍生物已被預測為穩定或介穩定的。根據目前已知的信息,除鋰之外的鹼金屬都能形成鹼化物。鹼化物的化學性質和電子鹽(一種以束縛電子為負離子的鹽)類似。由於擁有不同尋常的化學計量和低電離電位,鹼化物有很高的理論研究價值。
鋰離子(Li+)的半徑很小(76pm),會極化化合物中的陰離子,使化合物具有一定共價性;因此,鋰的化學性質和這一族中的其他元素有一些差異。例如,氟化鋰是唯一不溶於水的鹼金屬鹵化物;氫氧化鋰是唯一不潮解的鹼金屬氫氧化物。鋰和鎂存在對角線規則,鋰的某些化學性質和鎂相近。比如說,鋰可以形成穩定的氮化物,這一性質在鎂所在的鹼土金屬中很普遍,但在鹼金屬中則顯得獨特。此外,在各自所在的族中,只有鋰和鎂可以形成共價有機金屬化合物。
根據推測,鈁和其它鹼金屬也會有一些性質差異。鈁的原子量很高,它的電子運動較快,會引發更明顯的相對論效應,鈁具有的7s電子因而會更穩定。根據推測,鈁的電負性、電離能會比銫更高,這和鹼金屬從上到下電負性和電離能的變化趨勢相反。此外,鈁的原子半徑可能會反常地低。
影片