电极极化查看源代码讨论查看历史
| 电极极化 |
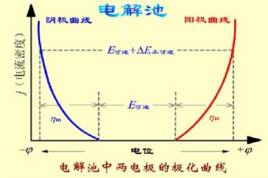 |
电极极化,在不可逆条件下,当有电流通过电极时,发生的是不可逆的电极反应,此时的电极电势与可逆电极电势会有所不同。电极在有电流通过时所表现的电极电势与可逆电极电势产生偏差的现象称为电极极化。电极极化的特征是:阴极电位比平衡电位更负(阴极极化),阳极电位比平衡电位更正(阳极极化)。
简介
在可逆电池的情况下,整个电池处于电化学平衡状态,两个电极也分别处于平衡状态,电极电位是由能斯特方程决定的,是平衡的电极电位。此时,通过电极的电流为零,即电极反应的速率为零。若要使一个不为零的电流通过电极,电极电位必须偏离平衡电极电位的值,这个现象就称为电极的极化。
电极极化(electrode polarization) 电子导体与围岩中溶液接触时,会形成电偶层,产生电位跳跃,这个电位跳跃便称为电子导体与溶液接触时的电极电位。当有外电场作用时,相对平衡的电极电位数值将发生变化。通常把在-定电流密度作用下的电极电位与相对平衡的电极电位的差值,称为电极极化。常见的有电化学极化、浓差极化等。由电极极化作用引起的电动势叫做超电压 。
评价
一个电极,在可逆情况下,电极上有一定的带电程度,建立了相应的电极电势jr。当有电流通过电极时,若电极一溶液界面处的电极反应进行得不够快,导致电极带电程度的改变,也可使电极电势偏离jr。以电极(Pt)H2(g)|H为例,作为阴极发生还原作用时,由于H变成H2的速率不够快,则有电流通过时到达阴极的电子不能被及时消耗掉,致使电极比可逆情况下带有更多的负电,从而使电极电势变得比jr低,这一较低的电势能促使反应物活化,即加速H转化成H2。当(Pt)H2(g)|H作为阳极发生氧化作用时,由于H2变成H的速率不够快,电极上因有电流通过而缺电子的程度较可逆情况时更为严重,致使电极带有更多的正电,从而电极电势变得比jr高。这一较高的电势有利于促进反应物活化,加速使H2变为H。将此推广到所有电极,可得具有普遍意义的结论:当有电流通过时,由于电化学反应进行的迟缓性造成电极带电程度与可逆情况时不同,从而导致电极电势偏离jr的现象,称为"活化极化"或"电化学极化"。电极发生活化极化时与发生浓差极化时一样,阴极电势总是变得比jr低,而阳极电势总是变得比jr高。因活化极化而造成的电极电势jI与jr之差的绝对值,称为"活化过电势"。活化过电势的大小是电极活化极化的量度 。[1]